Новое исследование ученых закладывает основу корректировки нейрологических болезней от эпилепсии до Альцгеймера
Ключевой элемент, отвечающий за равновесие между процессами торможения и возбуждения нервной системы человека обнаружили ученые Научно-исследовательского института общей патологии и патофизиологии (ФГБНУ «НИИОПП»). Этим элементом оказалась АТФаза, входящая в структуру ГАМКА- рецепторов — главных тормозных рецепторов в нервной системе. В будущем это позволит использовать АТФазу как молекулярную мишень для тестирования новых фармакопрепаратов против нейрологических расстройств — эпилепсии, аутизма, болезни Паркинсона и Альцгеймера.
Нервная система представляет собой сложно организованную систему клеток (нейронов). Они регулируют деятельность всего организма через передачу электрических импульсов. Происходит это за счет двух фундаментальных физиологических процессов — возбуждения и торможения трансмембранного потенциала (под этим термином понимается различие в электрическом потенциале внутри клетки и снаружи). Поддержание баланса (равновесия) между возбуждением/торможением обеспечивается работой расположенных в мембранах нейрональных клеток ионных каналов и транспортеров.
Главные тормозные рецепторы в нервной системе — это ГАМКА-рецепторы. В последние два десятилетия с помощью применения электрофизиологических, биохимических, флуориметрических и молекулярных методов (включая экспрессию рекомбинантного белка) ученые доказали, что некоторые ключевые подтипы ГАМКА-рецепторов энергозависимы и могут транспортировать ионы с отрицательным зарядом — хлор (Cl-) и бикарбонат (НСО3-), за счет использования энергии, высвобождающейся при расщеплении АТФ — главной энергетической молекулы в организме.
Свое открытие комментирует главный научный сотрудник НИИОПП, доктор биологических наук Сергей Мензиков: «Обнаружение в структуре ГАМКА- рецепторов АТФазной системы показало гораздо более сложную картину их функционирования, чем считалось раннее — наряду с пассивным переносом анионов Cl-/НСО3- в белковой структуре существует их активный транспорт. Такое открытие фундаментально меняло представление о функционировании ГАМКА- рецепторов и требовало дальнейших доказательств их двойственной природы на физиологическом уровне. Однако сложность в подтверждении этой гипотезы заключалась в многообразии уже известных подтипов ГАМКА-рецепторов, а также наличии в нейрональных мембранах и в рецепторной структуре различных систем (протеинкиназ или фосфатаз), молекулярный механизм функционирования которых связан с процессами гидролиза АТФ».
Ученым было необходимо найти особый методический подход, который позволил бы на физиологическом уровне отделить АТФ-зависимый транспорт анионов от их пассивной проницаемости через рецепторный канал.
В разработке такого методического подхода исследователи опирались на современные данные, демонстрирующие, что физиологическая функция ГАМКА- рецепторов регулируется большей частью через процессы их десенситизации — потери чувствительности, которые парадоксальным образом предотвращаются процессами их восстановления — ресенсибилизацией.
Именно нарушение молекулярных механизмов, за счет которых происходят процессы десенситизации/ресенситизации рецепторов, приводит к психическим расстройствам и наркомании. Однако сегодня наиболее изученными являются механизмы потери чувствительности, тогда как молекулярные события, запускающие процесс их восстановления, в основном остаются загадкой.
Сотрудникам института при использовании биофизического метода с применением ряда специфических препаратов, имитирующих различные состояния гидролиза АТФ, удалось доказать ключевую роль АТФазной системы в восстановлении концентрации анионов в нейронах после потери чувствительности. Это, в свою очередь, обеспечивает последующую эффективную активацию ГАМКА-рецептора.
Эти фундаментальные достижения позволили развить новое направление исследований в регуляции функции ГАМКА-рецепторов.
В течение трех лет ученые планируют показать структурные изменения, сопутствующие переключению от пассивного к активному транспорту анионов. Полученные результаты позволят в дальнейшем использовать обнаруженную АТФазу как молекулярную мишень для создания и тестирования новых фармакологических препаратов в доклинических исследованиях, а затем и в клинических испытаниях. Это расширит возможности корректировки таких серьезных неврологических нарушений, как эпилепсия, аутизм, болезнь Паркинсона и Альцгеймера.
Исследование выполнено при поддержке Минобрнауки России. Научная статья опубликована в международном журнале.
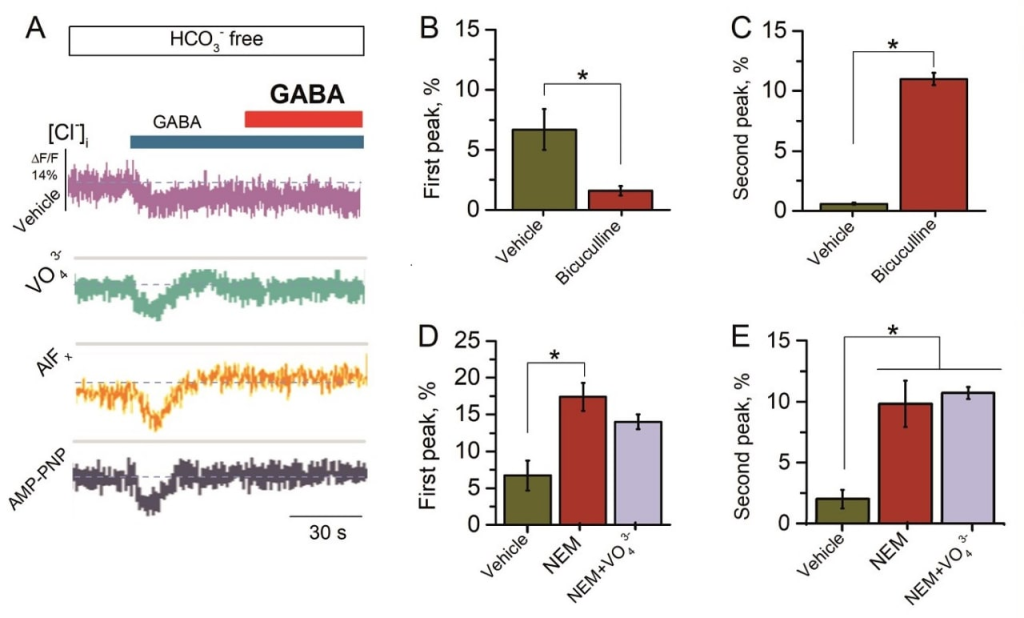
Рисунок: повторное применение ГАМК вызывает десенсибилизацию ГАМКАР-опосредованного входа Cl- в нейрональные клетки.






